Imunoterapia ganha força no tratamento contra o câncer pelo SUS
Lei inclui a imunoterapia nos protocolos da rede pública, e Instituto Butantan passará a produzir o medicamento pembrolizumabe
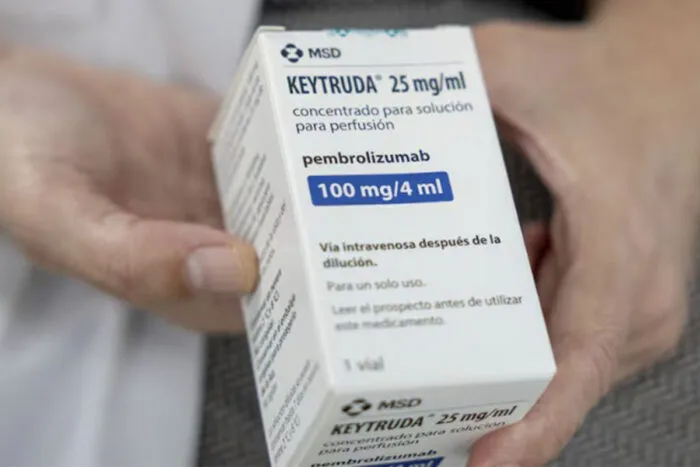
A Comissão de Oncologia Municipal não possui dados consolidados sobre o número de pacientes com câncer que utilizaram a imunoterapia como tratamento na rede pública nos últimos anos, e o pembrolizumabe – considerado um dos medicamentos oncológicos mais avançados para este fim -, não era ofertado rotineiramente pelo SUS em Juiz de Fora. Mas duas mudanças recentes em nível federal podem mudar essa realidade e facilitar o acesso a terapias modernas no município, na região da Zona da Mata mineira e pelo país afora. Em março, o Ministério da Saúde (MS) anunciou uma parceria para a produção 100% nacional do pembrolizumabe no SUS, junto com o Instituto Butantan e a farmacêutica Merck Sharp & Dohme (MSD), responsável pelo desenvolvimento do fármaco, comercializado como Keytruda. Já em abril, houve avanço com a Lei nº 15.379/2026, que acelera o acesso à imunoterapia na rede pública, quando houver comprovação de maior eficácia ou segurança em relação às terapias tradicionais, como quimio e radioterapia.
O pembrolizumabe foi incorporado no SUS em agosto de 2020 apenas para o tratamento de primeira linha do melanoma avançado não cirúrgico e metastático. Como os custos do medicamento importado são muito altos – no mercado privado, cada frasco do medicamento pode custar entre R$ 19 mil e R$ 27 mil, segundo o Conselho Federal de Farmácia – muitos pacientes com outros tipos de câncer recorrem à Justiça para acessar a imunoterapia, que ajuda o sistema imunológico a reconhecer e destruir células cancerígenas, reativando as células de defesa e fortalecendo a resposta imunológica contra a doença. “A incorporação (ao SUS) foi baseada em evidências científicas que apontam ganho de sobrevida e melhor controle da doença. A imunoterapia pode ser indicada como primeira linha em casos específicos, mas não substitui integralmente a quimioterapia, radioterapia ou cirurgia, cuja indicação depende da avaliação individual”, destaca o MS, acrescentando que a fabricação nacional permitirá ampliar o uso dessa imunoterapia de ponta para o tratamento de outros tipos de câncer na rede pública.
Ainda conforme o MS, atualmente, a Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (Conitec) analisa a ampliação do medicamento para outras quatro indicações: câncer de mama triplo negativo em estágio inicial de alto risco; câncer de pulmão de células não pequenas em estágio IV com alta expressão de PD-L1; carcinoma de esôfago avançado ou metastático com expressão de PD-L1; e câncer de colo do útero persistente, recorrente ou metastático com expressão de PD-L1. As análises seguem critérios de eficácia, segurança, custo-efetividade e impacto orçamentário. O prazo de decisão é de até 180 dias, prorrogáveis por mais 90. Em caso de incorporação, o prazo para oferta no SUS é de até 180 dias.
Saiba como acessar a imunoterapia pelo SUS
Questionada sobre os impactos dessas medidas na prática para pacientes oncológicos do SUS em Juiz de Fora, a Secretaria de Saúde Municipal avalia que a produção 100% nacional do pembrolizumabe e a Lei nº 15.379/2026 são avanços cruciais. “A ampliação da oferta via SUS trará benefícios fundamentais para os pacientes de Juiz de Fora, incluindo: melhora da sobrevida e qualidade de vida; acesso equitativo a tratamento de ponta.” A pasta não possui dados sobre o número de recursos judiciais ligados ao tema, mas reconhece a existência de casos de pacientes que buscaram o tratamento por via judicial para outros tipos de câncer não cobertos pelo SUS. “Contudo, a Secretaria de Saúde Municipal não dispõe de mensuração quantitativa específica desses casos judicializados.”
Ainda de acordo com a Prefeitura de Juiz de Fora (PJF), o acesso oncológico segue as diretrizes nacionais, com avaliação por equipes especializadas em Centros de Assistência de Alta Complexidade em Oncologia (Cacons) e em Unidades de Assistência de Alta Complexidade em Oncologia (Unacons).
O Ministério da Saúde reforça que, para acesso ao tratamento, o paciente deve ser atendido na rede pública e encaminhado a um hospital habilitado em oncologia (Cacon ou Unacon). Após avaliação, conforme os protocolos clínicos, o tratamento é autorizado – via Autorização de Procedimentos de Alta Complexidade (Apac) – e realizado no próprio serviço especializado. “O financiamento dessas terapias está em processo de modernização com a criação do Componente da Assistência Farmacêutica em Oncologia (AF-Onco), cuja implementação ocorrerá de forma gradual. Até lá, permanece o fluxo atual de atendimento.”
Desafios da imunoterapia
O Movimento Todos Juntos Contra o Câncer (TJCC), que congrega representantes de diferentes setores voltados ao cuidado do paciente com câncer, avalia que a sanção da Lei nº 15.379/2026 representa avanço relevante, ao alinhar o país às melhores práticas internacionais e fortalecer diretrizes já estabelecidas. “No entanto, sua efetividade dependerá diretamente da capacidade de implementação concreta no âmbito do SUS, especialmente no que diz respeito ao financiamento adequado, à atualização tempestiva dos PCDTs (Protocolo Clínico e Diretrizes Terapêuticas) e à articulação federativa para garantir o acesso equitativo aos tratamentos.”
Para o TJCC, é fundamental que a regulamentação estabeleça fluxos claros, com o suporte técnico da Conitec, para assegurar a disponibilização dessas terapias na ponta, “contribuindo para a redução das desigualdades regionais e promovendo um modelo de cuidado mais eficiente, custo-efetivo e centrado no bem-estar do paciente oncológico”.
Segundo o Ministério da Saúde, a Parceria para o Desenvolvimento Produtivo (PDP), com o Instituto Butantan e a MSD, para transferência de tecnologia do pembrolizumabe está na fase II, com treinamentos e preparação para produção nacional do medicamento, para que o produto possa ser adquirido pelo SUS, na fase III. A transferência da tecnologia deve ocorrer ao longo de até 10 anos, para que o Instituto Butantan incorpore a capacidade produtiva.
“A iniciativa também representa um passo importante para a autonomia do setor farmacêutico brasileiro. Além de facilitar o acesso à imunoterapia, a produção local pode contribuir para a redução da judicialização na saúde, ao permitir que tratamentos inovadores estejam disponíveis de forma mais ampla e equitativa para a população”, enfatiza o Conselho Federal de Farmácia.