Reino Unido autoriza a realização de terapia gênica inédita para pessoas com anemia falciforme
Técnica usa a tecnologia de edição genética CRISPR/Cas9, que manipula as células em laboratório e as devolve ‘corrigidas’ para o corpo do paciente
A Agência Reguladora de Medicamentos e Produtos para a Saúde (MHRA) do Reino Unido concedeu autorização condicional para a primeira terapia gênica do mundo no tratamento da anemia falciforme. Essa concessão, feita em casos específicos e com dados menos abrangentes de estudos clínicos, ocorre quando os benefícios imediatos superam os riscos. A expectativa é que essa autorização se torne definitiva assim que a farmacêutica responsável apresentar estudos mais amplos.
A terapia, batizada de Casgevy, foi desenvolvida em parceria pelas empresas farmacêuticas Vertex e CRISPR Therapeutics. Ela utiliza a tecnologia CRISPR/Cas9, uma técnica de edição gênica que realiza cortes precisos no DNA do paciente. O objetivo é tratar a anemia falciforme, uma condição considerada rara, apesar de ser uma das doenças genéticas mais comuns e conhecidas globalmente.
A autorização para o uso da Casgevy foi concedida a pacientes com mais de 12 anos que apresentem crises vaso-oclusivas recorrentes (entupimento dos vasos sanguíneos, causando dor intensa) e para os quais o transplante de medula óssea seja indicado, mas não haja um doador compatível disponível. A agência reguladora também aprovou a mesma terapia para pacientes com talassemia beta, outra doença hereditária, que sejam dependentes de transfusão sanguínea e não tenham conseguido encontrar um doador compatível para o transplante de medula.
Segundo a farmacêutica Vertex, em dois ensaios clínicos globais, a terapia gênica alcançou os resultados primários esperados, livrando os pacientes de crises vaso-oclusivas graves e tornando-os livres de transfusões de sangue por 12 meses consecutivos. Espera-se que esses resultados perdurem pelo resto da vida. Em comunicado, a empresa informou que está trabalhando com as autoridades de saúde para garantir o acesso dos pacientes elegíveis o mais rápido possível. A mesma terapia está sob análise da FDA (agência norte-americana reguladora de fármacos e alimentos), e a decisão deve ser anunciada em dezembro.
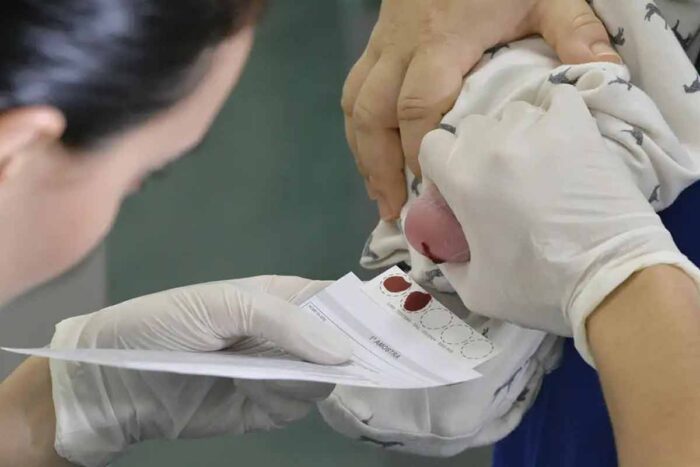
O que é a anemia falciforme?
A anemia falciforme é uma alteração genética que ocorre em um dos componentes da hemoglobina, a chamada beta-globina, uma proteína presente nas hemácias, células essenciais para o transporte de oxigênio para os órgãos e tecidos. Enquanto as hemácias de um paciente saudável são arredondadas e circulam facilmente pelos vasos sanguíneos, as de um paciente com a doença são endurecidas e assumem a forma de uma foice (ou lua minguante) quando há diminuição da oxigenação. Além disso, elas se rompem mais facilmente e têm uma vida útil mais curta do que as hemácias saudáveis.
Outro problema decorrente dessa alteração nos glóbulos vermelhos é que, devido ao seu formato de foice (daí o nome anemia falciforme), eles tendem a se aglomerar e aderir às paredes dos vasos sanguíneos. Isso resulta em crises vaso-oclusivas, obstruções que podem causar dor intensa e aumentar o risco de eventos cardiovasculares, como insuficiência cardíaca, síndrome torácica aguda, acidente vascular cerebral, entre outros.
A doença é extremamente debilitante, com um profundo impacto social e emocional. Os pacientes enfrentam hospitalizações frequentes, o que muitas vezes os leva a se afastarem do trabalho. Além das crises de dor intensa, a condição pode resultar em casos de anemia crônica, tornando os pacientes dependentes de transfusões de sangue. Adicionalmente, alguns indivíduos sofrem de priapismo, uma ereção involuntária e duradoura do pênis, que não apenas causa dor intensa, mas também constrangimentos significativos para o paciente. Mesmo com tratamento médico, a expectativa de vida das pessoas com anemia falciforme pode ser reduzida em até 20 anos em comparação com aqueles sem a doença.
A anemia falciforme teve sua origem na África e é mais comum em pessoas afrodescendentes, embora possa afetar qualquer indivíduo. Para desenvolver a doença, é necessário herdar dois genes alterados, um do pai e outro da mãe; caso contrário, a pessoa terá apenas o traço falciforme. O tratamento padrão oferecido pelo Sistema Único de Saúde (SUS) no Brasil inclui o uso de medicamentos profiláticos para infecções bacterianas, especialmente importante em crianças, que ficam mais suscetíveis a infecções devido à disfunção no baço. Envolve, ainda, o uso de medicamentos opiáceos e anti-inflamatórios para lidar com a dor aguda crônica, transfusões de sangue, quelantes de ferro e o uso de um medicamento especializado chamado hidroxiureia.
Além disso, o transplante de medula óssea já é uma realidade para essas pessoas, sendo inclusive oferecido pelo SUS. No entanto, a dificuldade está em encontrar um doador de medula compatível. Segundo dados do Ministério da Saúde, no ano passado, 20 pacientes realizaram o transplante de medula na rede pública. Neste ano, até outubro, foram registrados 15 pacientes submetidos ao procedimento. Apesar dos avanços e da disponibilidade pelo SUS, esse número ainda é bastante reduzido diante da quantidade de pessoas afetadas pela doença. Segundo a Federação Nacional das Associações de Pessoas com Doença Falciforme (FENAFAL), cerca de 200 pacientes realizaram o transplante na rede suplementar.
Embora seja classificada como uma doença rara globalmente, estima-se que entre 60 mil e 100 mil pessoas tenham anemia falciforme no Brasil. A abrangência da doença é tão significativa que, no mês passado, o Ministério da Saúde anunciou a sua inclusão como notificação compulsória. Isso implica que, assim que o paciente receber o diagnóstico por meio do teste do pezinho, o serviço de saúde será obrigado a informar ao governo. Até então, as crianças eram diagnosticadas ao nascer, mas nem sempre esses dados eram comunicados ao ministério.
“Essa atitude do governo é essencial para sabermos exatamente onde estão esses pacientes para que sejam realizadas ações de saúde pública, como criação de mais centros especializados para esse atendimento”, disse Elvis Silva Magalhães, coordenador científico da Fenafal – entidade que representa mais de 30 mil pacientes no Brasil. Magalhães tem a doença e foi um dos primeiros pacientes a serem submetidos ao transplante de medula no Brasil, em 2005, quando o tratamento ainda era considerada experimental.
- LEIA MAIS sobre Ciência e Tecnologia.
O que faz a terapia gênica?
A terapia gênica é a grande promessa de cura – senão a cura, pelo menos o desaparecimento quase total dos sintomas – para os pacientes com anemia falciforme. No caso da terapia desenvolvida pela Vertex, os cientistas usam a edição genética para religar o gene da gama-globina (hemoglobina fetal), que é substituído pela beta-globina (hemoglobina adulta) à medida em que crescemos.
A ideia é bastante complexa. Após o nascimento, o gene da gama-globina é “desligado” do organismo e o gene da beta-globina começa a funcionar, resultando na troca da hemoglobina fetal pela hemoglobina adulta. Como as pessoas com anemia falciforme têm o gene da beta-globina disfuncional, os sintomas da doença surgem justamente nesse período, quando a criança ainda é um bebê.
Os cientistas passaram a perceber que algumas pessoas tinham o gene defeituoso da beta-globina, mas não desenvolviam os sintomas falciformes. Após anos de estudo, eles descobriram que o gene da gama-globina (a hemoglobina fetal) nessas pessoas não era desligado após o nascimento e continuava ativo. Ou seja: a hemoglobina fetal era uma excelente substituta da hemoglobina adulta.
A partir dessa descoberta, havia uma oportunidade de tratar (ou curar) a doença: encontrar uma forma de fazer com que o gene da gama-globina continuasse ativo ao longo da vida das pessoas com anemia falciforme.
E foi isso que a Vertex e a CRISPR Therapeutics fizeram: uma manipulação genética (uma religação do gene da gama-globina) capaz de permitir a volta da produção de hemoglobina fetal. Parece simples, mas não é. Para que isso aconteça, os cientistas precisam coletar as células-tronco da medula óssea do paciente, editar o gene em laboratório usando a técnica CRISPR/Cas9, e depois devolvê-las ao paciente para que a medula óssea passe a produzir células saudáveis. O processo é muito parecido com o transplante de medula convencional – a diferença é que usa as células do próprio paciente e não depende de doador compatível.
“Doenças monogênicas, como talassemia beta maior e anemia falciforme, podem ser melhoradas e talvez até curadas com terapia genética. Existem estudos em andamento de diferentes métodos e abordagens. A tecnologia de edição por CRISPR/Cas9 é uma excelente opção e vai ajudar muito os pacientes”, disse hematologista Nelson Hamerschlak, coordenador da Unidade de Transplante de Medula Óssea do Hospital Israelita Albert Einstein, que já fez cerca de 20 transplantes de medula em pacientes com anemia falciforme.
“Por enquanto, a terapia foi liberada somente para quem não tem doador de medula, mas creio que, no futuro, com a maior experiência, ela poderá substituir o transplante de medula óssea alogênico [que utiliza células de um doador]”, afirmou o hematologista.
Pesquisa no Brasil
No Brasil, o tratamento ainda não está disponível, mas a equipe da Iniciativa Einstein em Terapia Gênica do Hospital Israelita Albert Einstein está conduzindo uma pesquisa desde 2019 em busca de uma alternativa de terapia gênica para pessoas com anemia falciforme. A pesquisa é realizada por meio de uma parceria entre o hospital e o Ministério da Saúde, com o Programa de Apoio ao Desenvolvimento Institucional do SUS (Proadi-SUS).
Segundo Ricardo Weinlich, cientista líder do grupo, o time está pesquisando diferentes estratégias – a primeira é tentar corrigir diretamente a mutação genética causadora da doença no gene da beta-globina.
“Nessa primeira estratégia, testamos um conjunto de ferramentas para corrigir essa mutação em laboratório. Os resultados que alcançamos ainda são mistos. Apesar de serem promissores, no momento ainda não conseguimos afirmar se vai funcionar em maior escala e se há eficácia e segurança para partirmos para o ensaio clínico”, explicou Weinlich.
Em paralelo à tentativa de correção da alteração genética, o grupo passou a testar também uma ferramenta mais moderna, chamada editor de base, para aumentar a expressão da hemoglobina fetal (assim como fez a Vertex).
“Estamos em constante diálogo e atualização com o Ministério da Saúde. Se a primeira estratégia não der certo, paralelamente já estamos buscando uma segunda opção. Ainda estamos bem no começo, mas o fato de o Brasil estar desenvolvendo uma terapia desse porte e que poderá ser oferecida pelo SUS é importante do ponto de vista de autonomia e soberania nacional, além de ser uma grande oportunidade de redução de custos no futuro”, afirmou o pesquisador.
O altíssimo custo da terapia gênica, estimado atualmente na casa dos milhões de dólares por paciente, representa um dos fatores limitantes, ainda distante da realidade dos serviços de saúde. Mesmo assim, a notícia da aprovação foi recebida com entusiasmo tanto pelos cientistas quanto pelas associações de pacientes.
“Estamos muito entusiasmados com essa notícia. A primeira vez que eu ouvi sobre terapia gênica para anemia falciforme foi em 2015. Parecia algo muito distante, mas se transformou em realidade. Os custos são altos sim, mas quanto custava um transplante de medula na década de 70? Certamente também era caríssimo e hoje ele é uma alternativa acessível, inclusive para pacientes do SUS. Ciência é isso. Vemos com muita esperança essa terapia”, comemorou Magalhães.